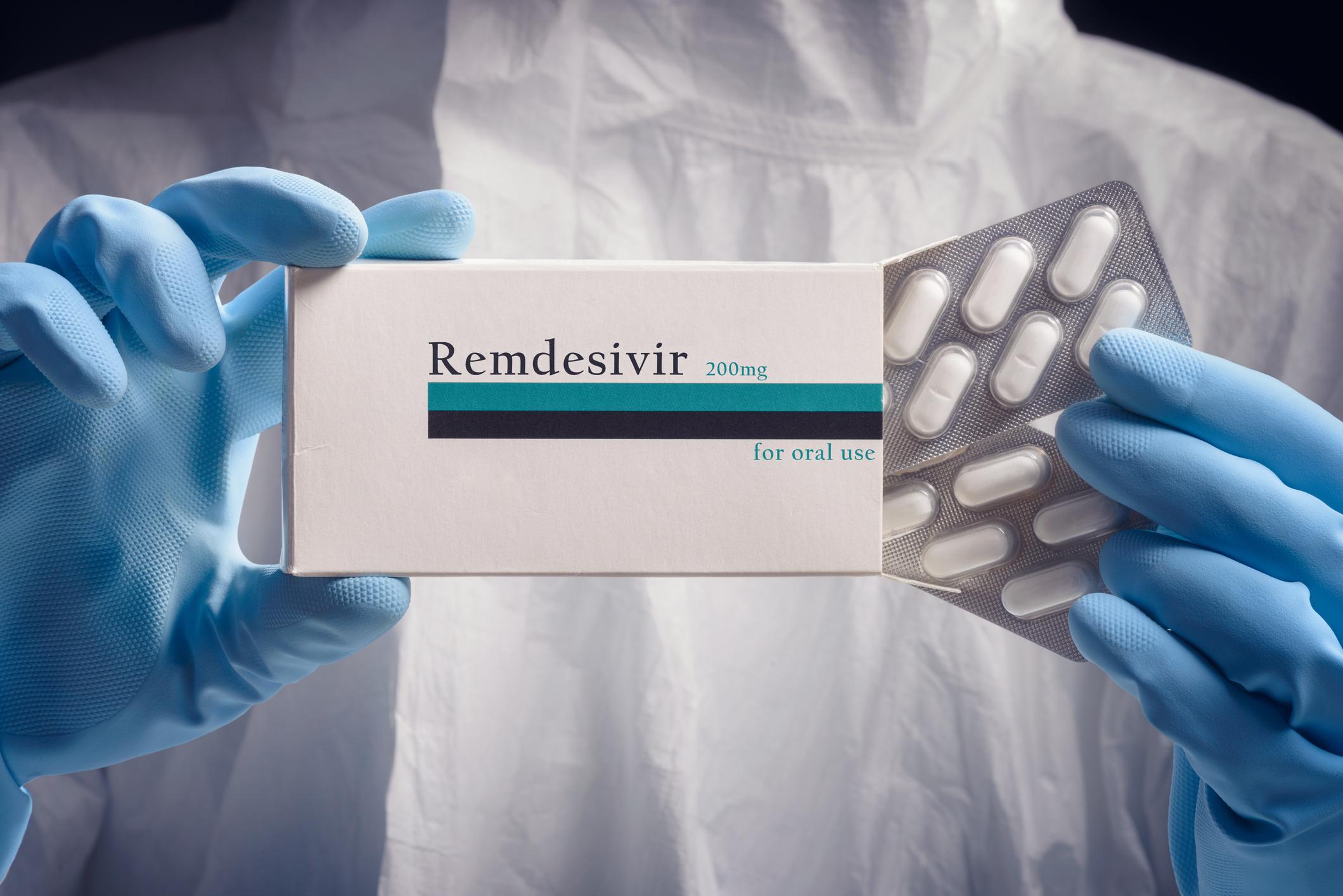
L’Europa nella gestione della Pandemia ha commesso una serie di errori che sono sotto gli occhi di tutti, dalla prevenzione ai contratti sui vaccini; un fallimento evidente. Ma quanto emerge da alcune carte scoperte a Bruxelles è un probabile spreco da un miliardo di euro. Uno spreco che si gioca in meno di 24 ore. Protagonista il Remdesivir, il farmaco che nella prima fase veniva considerato utile (pur tra mille perplessità).
L’8 ottobre 2020 la Commissione Europea infatti ha firmato un contratto con Gilead Sciences per 500000 dosi endovenose dell’antivirale Remdesivir dal valore di 2000 euro l’una, per un totale di 1,035 miliardi di euro.
Il giorno dopo, il 9 ottobre 2020, veniva pubblicato lo studio “Solidarity” che dimostrava, dati alla mano, come il Remdesivir fosse inefficace contro il Covid. In pratica l’Europa ha acquistato per 1 mld di euro un farmaco proprio poche ore prima che diventasse ufficialmente inutile secondo il mondo scientifico. Possibile che nessuno sapesse nulla? Possibile che nessuno si sia informato? Possibile che l’Ema non fosse a conoscenza (ed i dubbi sul Remdesivir erano già noti anche se non ancora dimostrati)?
A sollevare la questione un gruppo di europarlamentari francesi che hanno depositato la seguente interrogazione il 30 novembre 2020.
“All’epoca, Gilead non poteva ignorare le prove convincenti sull’inefficacia della molecola contro la mortalità causata dal Covid-19. Secondo la rivista Science Gilead è stato informato dall’OMS il 23 settembre 2020 dei risultati negativi di uno studio condotto in 405 ospedali di 30 paesi su 11000 pazienti Covid-19. L’UE ha ricevuto le informazioni il 9 ottobre 2020. Possibile che nessuno sapesse nulla 24 ore prima? Il professor Didier Raoult ha denunciato le pressioni di Gilead. L’OLAF indaga su frodi ai danni del bilancio dell’UE, scandali di corruzione e gravi comportamenti scorretti nelle istituzioni europee. Può la Commissione chiedere all’OLAF di avviare un’indagine sulla falsificazione, occultamento e adulterazione delle informazioni fornite alla Commissione da Gilead?
Intende la Commissione chiedere all’OLAF di avviare un’indagine sulle violazioni o sui conflitti di interesse relativi al Remdevisir presso i servizi e le agenzie dell’UE competenti o le autorità nazionali?”
La mancata reazione dell’EMA e la sospensione dell’autorizzazione condizionale del 3 luglio 2020 due mesi dopo che Gilead era stata informata dei risultati negativi; nessuno studio di efficacia post-autorizzazione è stato incluso nel piano di gestione del rischio; monitoraggio inadeguato dell’azienda; nessuna riunione del CHMP dedicata a ottobre o novembre 2020.
A rispondere il 26 marzo 2021 (4 mesi dopo) è Stella Kyriakides, la commissaria europea per la salute e la sicurezza alimentare:
“Il contratto firmato con Gilead riguarda il prodotto Veklury Remdevisir in possesso di un’autorizzazione all’immissione in commercio condizionata valida. L’Agenzia europea per i medicinali (EMA) ha chiesto l’accesso ai dati della Solidarity Trial. L’EMA valuterà le prove, insieme ad altri dati pertinenti, per verificare se siano necessarie modifiche all’autorizzazione all’immissione in commercio di Veklury nell’UE.
Nell’ambito del contratto quadro che la Commissione ha concluso con Gilead, gli Stati membri e gli altri paesi che hanno firmato l’accordo di aggiudicazione congiunta , se lo desiderano, possono ordinare il Remdesivir. Non vi è alcun obbligo di acquisto. L’importo dichiarato è pertanto un importo massimo che potrebbe essere speso dai paesi, non si tratta di un importo che la Commissione ha pagato.”
A riguardo dell’accordo con l’UE, la società Gilead ha confermato alla rivista scientifica “Science” che l’OMS a fine settembre ha fornito alla società un manoscritto sui risultati dello studio, ma un portavoce della Commissione europea, ha affermato che questi risultati non sono stati rivelati durante i negoziati.
E’ evidente quindi che da una parte la casa farmaceutica pare essersi fatta pochi scrupoli, tenendo per se alcune informazioni ufficiali sul farmaco ricevuto persino dall’Oms. Dall’altra però pare poco credibile che la Commissione Europa potesse “non sapere” nulla sulla questione.
Inutile poi sperare di poter capire chi abbia sbagliato a Bruxelles. Nessuno infatti, a parte l’interrogazione parlamentare, ha deciso di fare il passo successivo, chiedendo l’apertura di una Commissione d’inchiesta
Sulla procedura e l’efficacia infatti un europarlamentare ci ha spiegato: “Le commissioni d’inchiesta hanno poteri limitati. È inutile chiederne l’istituzione che con molta probabilità non verrà concessa.”
“Il Remdesivir – spiega il Prof. Gabriele Costantino, chimico farmaceutico dell’Università di Parma – è un antivirale sintetizzato usato da 15 anni. È stato utilizzato nel trattamento dell’ebola e ha dimostrato una certa attività contro Sars e Sars-Cov-2. È stato somministrato per uso compassionevole, tuttavia successivi studi clinici non hanno mostrato nessun effetto sulla riduzione di mortalità ed un modesto miglioramento nei tempi di ospedalizzazione per alcune categorie di pazienti ricoverati. Aifa non ha mai detto quanto ha concordato per il farmaco. Mentre negli Stati Uniti un trattamento di 5 giorni costa circa 3200 dollari. La proposta di acquisto dell’Unione Europea è comprensibile dal punto di vista dell’emergenza ma alla luce degli studi clinici che erano già disponibili al momento della firma dell’accordo e resi pubblici subito dopo è stata quantomeno affrettata”.